5月14日,中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所錢(qián)友存研究組,聯(lián)合中國(guó)科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心宋昕陽(yáng)研究組,在Nature雜志在線(xiàn)發(fā)表了題為“Targeting symbionts by apolipoprotein L proteins modulates gut immunity”的研究成果。該研究首次揭示了小鼠腸道上皮細(xì)胞(Intestinal epithelial cells, IECs)分泌的載脂蛋白APOL9a/b及其人源同源蛋白APOL2可特異性識(shí)別擬桿菌目(Bacteroidales)細(xì)菌,誘導(dǎo)其釋放外膜囊泡(Outer membrane vesicles, OMVs),并激活宿主免疫因子IFN-γ-MHC-II信號(hào)通路,從而提升腸道黏膜屏障的抗感染能力。這項(xiàng)研究揭示了宿主免疫系統(tǒng)通過(guò)精細(xì)機(jī)制調(diào)控腸道微生態(tài)平衡,拓展了對(duì)宿主與共生菌共同進(jìn)化互作機(jī)制的理解,為菌群相關(guān)疾病的精準(zhǔn)干預(yù)與治療策略創(chuàng)新奠定了理論基礎(chǔ)。
哺乳動(dòng)物腸道是宿主與共生微生物互作的核心界面。腸道微生物來(lái)源的代謝產(chǎn)物(如膽汁酸、短鏈/長(zhǎng)鏈脂肪酸)及膜結(jié)構(gòu)分子(如多糖A、α-半乳糖神經(jīng)酰胺)等生物活性小分子可跨越腸道上皮屏障,進(jìn)而調(diào)控宿主免疫細(xì)胞分化與功能。例如,誘導(dǎo)結(jié)腸調(diào)節(jié)性T細(xì)胞(Regulatory T cells, Tregs)分化或促進(jìn)小腸上皮內(nèi)淋巴細(xì)胞(Intraepithelial lymphocytes, IELs)的聚集。與此同時(shí),宿主則通過(guò)上皮黏液屏障、抗菌蛋白(Anti-microbial peptides, AMPs)、分泌型免疫球蛋白(Secretory immunoglobulin A, sIgA)及補(bǔ)體成分(如Complement 3,C3)等防御機(jī)制維持菌群穩(wěn)態(tài)。然而,現(xiàn)有研究主要聚焦于廣譜性、非特異性的防御策略,對(duì)于宿主是否具備選擇性識(shí)別并調(diào)控特定共生菌群成員的能力仍缺乏深入理解。
為了系統(tǒng)挖掘宿主調(diào)控腸道菌群的關(guān)鍵分子,研究人員首先借助高通量蛋白質(zhì)組學(xué)技術(shù),對(duì)常規(guī)飼養(yǎng)(Conventional raised, CR)小鼠和無(wú)菌(Germ-free, GF)小鼠回腸黏液層中的蛋白質(zhì)組成進(jìn)行了全面對(duì)比分析。通過(guò)篩選菌群依賴(lài)性表達(dá)上調(diào)的蛋白質(zhì),并利用CR小鼠中回腸共生菌群結(jié)合蛋白的蛋白質(zhì)組進(jìn)行聯(lián)合分析,研究人員最終聚焦于一類(lèi)此前功能未明的脂蛋白家族成員——Apolipoprotein L9a/b(APOL9a/b, 或APOL9),并確認(rèn)其表達(dá)受菌群調(diào)控。同時(shí),單細(xì)胞測(cè)序及免疫熒光分析顯示APOL9a/b主要來(lái)源于腸上皮吸收細(xì)胞(Enterocyte)。為探明其靶向的共生菌是否具有微生物系統(tǒng)發(fā)育特異性,團(tuán)隊(duì)進(jìn)一步結(jié)合流式細(xì)胞分選技術(shù)與16S rRNA基因測(cè)序技術(shù),創(chuàng)建了“APOL9-seq”策略,并對(duì)APOL9蛋白結(jié)合的腸道微生物進(jìn)行了全面分析。研究結(jié)果顯示,無(wú)論是在小鼠還是在人源微生物結(jié)合實(shí)驗(yàn)體系中,APOL9a/b及其人類(lèi)同源物APOL2都表現(xiàn)出極強(qiáng)的群體選擇性,幾乎專(zhuān)一性地識(shí)別并結(jié)合擬桿菌目(Bacteroidales)細(xì)菌。
那么,APOL9/APOL2是如何實(shí)現(xiàn)對(duì)擬桿菌目細(xì)菌“精準(zhǔn)鎖定”的呢?研究人員猜測(cè)擬桿菌目細(xì)菌特有的細(xì)胞膜鞘脂組分可能介導(dǎo)該識(shí)別過(guò)程。隨后,研究人員通過(guò)選取擬桿菌屬的代表共生菌——多形擬桿菌(B.thetaiotaomicron)作為模式菌株,并利用基因編輯技術(shù)成功敲除其多個(gè)鞘脂生物合成相關(guān)基因。實(shí)驗(yàn)發(fā)現(xiàn),APOL9/2蛋白對(duì)B. thetaiotaomicron的結(jié)合能力依賴(lài)于其細(xì)胞膜上的一類(lèi)特殊脂質(zhì)——神經(jīng)酰胺-1-磷酸(Ceramide-1-phosphates, Cer1Ps)。一旦敲除Cer1P合成關(guān)鍵酶,APOL9/2與擬桿菌的結(jié)合能力明顯下降,表明Cer1P是介導(dǎo)其識(shí)別的關(guān)鍵分子。這一結(jié)果首次揭示,宿主可通過(guò)識(shí)別共生菌特有脂質(zhì)結(jié)構(gòu),從而精準(zhǔn)“靶向”特定微生物群落。
有別于傳統(tǒng)抗菌肽直接殺菌的方式,APOL9在生理濃度下與擬桿菌結(jié)合后并不引發(fā)細(xì)胞死亡,而是以一種非致死性的方式誘導(dǎo)這些革蘭氏陰性菌釋放大量外膜囊泡OMVs。這些OMVs直徑在幾十至數(shù)百納米之間,富含細(xì)菌來(lái)源的脂類(lèi)、蛋白和多糖等成分,因而可被宿主先天免疫系統(tǒng)識(shí)別并激活相應(yīng)通路。功能實(shí)驗(yàn)進(jìn)一步表明,這些由APOL9誘導(dǎo)產(chǎn)生的OMVs不僅能被宿主樹(shù)突狀細(xì)胞(Dendritic cell,?DC)捕獲,還能有效增強(qiáng)黏膜區(qū)域的IEC-T細(xì)胞互作介導(dǎo)的免疫反應(yīng)。具體而言,它們通過(guò)激活干擾素-γ(IFN-γ)信號(hào)通路,顯著提升小腸上皮細(xì)胞中MHC II類(lèi)分子的表達(dá)水平,從而促進(jìn)腸道上皮間一類(lèi)具有重要免疫調(diào)節(jié)功能的CD4?CD8αα? ?IEL的發(fā)育和維持。在體內(nèi)功能驗(yàn)證層面,研究團(tuán)隊(duì)構(gòu)建了Apol9a/b雙敲除小鼠模型,并發(fā)現(xiàn)其小腸上皮的MHC-II分子及CD4?CD8αα? IEL水平均發(fā)生下調(diào),且這一調(diào)控現(xiàn)象依賴(lài)于小鼠腸道擬桿菌的存在。同時(shí),在沙門(mén)氏菌(Salmonella typhimurium)經(jīng)口感染實(shí)驗(yàn)中,研究人員也發(fā)現(xiàn)APOL9缺失小鼠不僅腸道局部病原負(fù)載顯著升高,而且細(xì)菌易擴(kuò)散至肝臟、脾臟等內(nèi)臟器官,表現(xiàn)出更高的系統(tǒng)性感染風(fēng)險(xiǎn)和死亡率。相反,當(dāng)給予這些小鼠擬桿菌來(lái)源的OMVs時(shí),宿主的各項(xiàng)腸道免疫防御指標(biāo)也顯著提升,因而其感染癥狀也得到明顯緩解。
這項(xiàng)研究不僅首次揭示了一類(lèi)宿主新型載脂蛋白如何通過(guò)特異性識(shí)別共生菌膜脂分子并誘導(dǎo)其釋放具有免疫調(diào)節(jié)活性OMVs的因果機(jī)理,還為我們理解宿主如何“主動(dòng)塑造”腸道微生態(tài)提供了新的理論框架,同時(shí)也為開(kāi)發(fā)下一代基于菌群精準(zhǔn)調(diào)控的免疫干預(yù)手段奠定了分子基礎(chǔ)。
中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所副研究員楊濤、博士研究生胡孝虎,與中國(guó)科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心博士研究生曹飛為論文的共同第一作者。中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所錢(qián)友存研究員和中國(guó)科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心宋昕陽(yáng)研究員為文章共同通訊作者。該工作得到哈佛大學(xué)醫(yī)學(xué)院Dennis L. Kasper教授、清華大學(xué)醫(yī)學(xué)院梁冠翔教授、中國(guó)科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心石建濤研究員、中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所胡國(guó)宏研究員的支持和幫助。該工作得到了科技部國(guó)家重點(diǎn)研發(fā)計(jì)劃項(xiàng)目、國(guó)家自然科學(xué)基金委、中國(guó)科學(xué)院B類(lèi)先導(dǎo)專(zhuān)項(xiàng)、中國(guó)科學(xué)院“未來(lái)伙伴網(wǎng)絡(luò)專(zhuān)項(xiàng)”及上海市科委項(xiàng)目的資助。 該工作同時(shí)獲得中國(guó)科學(xué)院上海營(yíng)養(yǎng)與健康研究所所級(jí)公共技術(shù)中心,中國(guó)科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心生信平臺(tái)、化學(xué)生物學(xué)平臺(tái),中國(guó)科學(xué)院腦科學(xué)與智能技術(shù)卓越創(chuàng)新中心電鏡平臺(tái),中國(guó)科學(xué)院上海免疫與感染研究所動(dòng)物平臺(tái),上海交通大學(xué)流式平臺(tái),中科脂典公司及諾米代謝公司等多家單位、企業(yè)的技術(shù)支持。
論文鏈接:https://doi.org/10.1038/s41586-025-08990-4
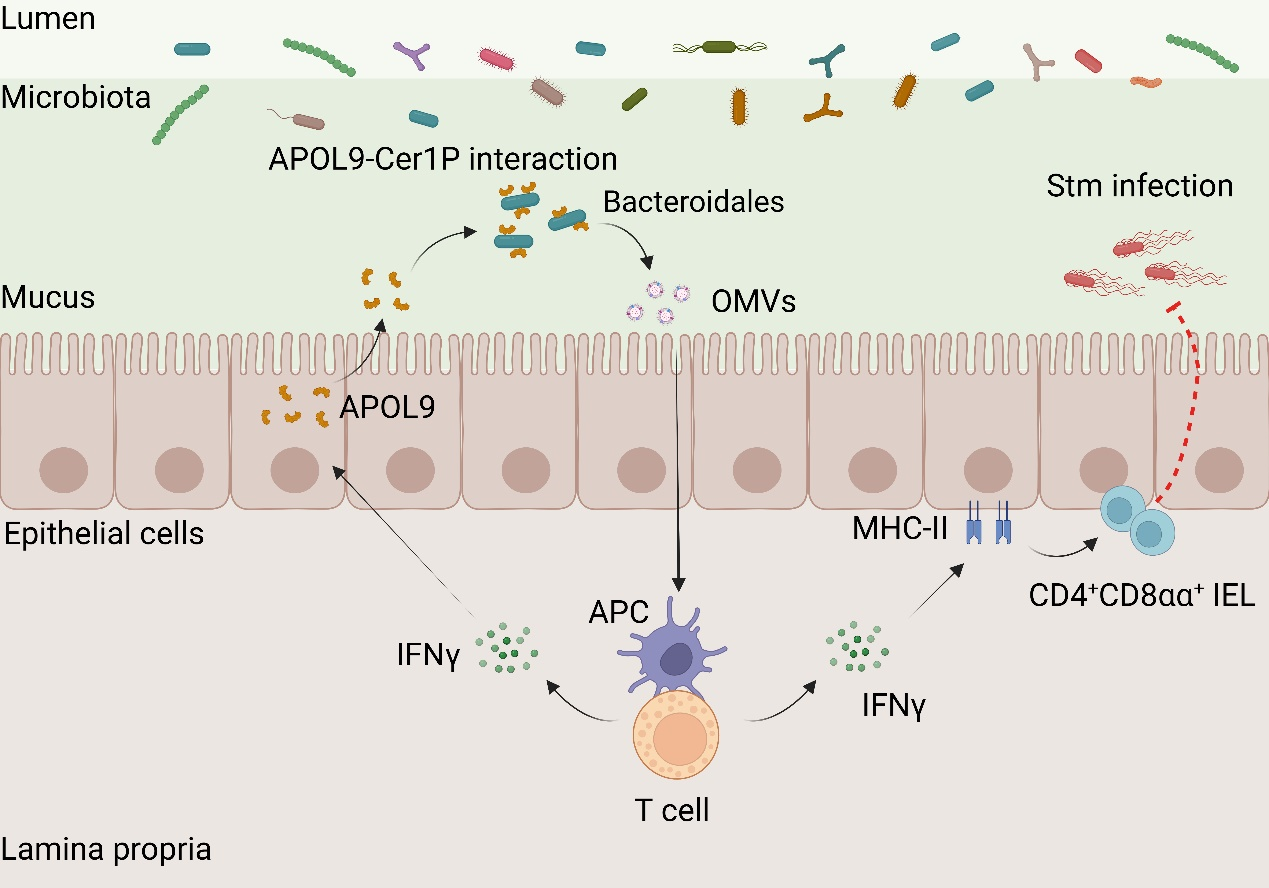
圖:新型載脂蛋白APOL9通過(guò)結(jié)合擬桿菌Cer1P分子誘導(dǎo)OMVs釋放并激活I(lǐng)FN-γ-MHC-II通路以增強(qiáng)腸道黏膜免疫